Энергетическое строение атома водорода. Постулаты Бора и объяснение происхождения линейчатых спектров
Теория основана на хорошо известном факте «превращения» фотона с энергий 1 МэВ в пару электрон – позитрон. Необходимо предупредить, что имеется замечательное совпадение: энергия фотона почти точно соответствует существующему определению классического радиуса электрона:
R e = ξ (e 0 2 / m e c 2) = 2,81794334·10 –15 [m ],
а энергия m e c 2 ≈ 0,5MeV . Совпадение порождает естественное подозрение на использование автором тавтологии, не имеющей физического смысла. Но это не так в силу опытного факта превращения фотона в пару электрон – позитрон. В статье получена электрическая безмассовая структура физического вакуума с дипольным расстоянием r e = 1,3987632·10 –15 [m ] и предельно возможная деформация диполя Δr rb = 1,02072687·10 –17 [m ], удвоенная сумма которых точно равна классическому радиусу электрона. Причина в том, что энергия фотона «красной границы» для вакуума в 2 раза больше энергии масс электрона и позитрона.
Другим важным обстоятельством гипотезы о природе гравитации есть то, что причиной притяжения всех тел друг к другу является слабая разность элементарных зарядов (+) и (–) в диполе. По законам индукции Фарадея и сил Кулона все тела притягиваются друг к другу поляризуемым зарядом дипольной структуры среды, а свойства инерции заключается в свойстве среды сопротивляться любым ускорениям материальных тел.
Эта исключительно важная среда существования вещества в природе позволила опубликовать статью , которую можно принять как частную программу развития физических знаний об устройстве природы.
Модель атома водорода по Н. Бору
Обратимся к истокам начал квантовой механики, положенным Н. Бором (1885...1962) в форме модели атома водорода, которая получила блестящее подтверждение в спектральных исследованиях излучения водорода. Кратко напомним основные положения работы Н. Бора.
Энергия Е электрона в атоме, исходя из классической физики, складывается из кинетической энергии Т и потенциальной электрической энергии U : Е = Т + U . Отметим, что в область микромира вторглась классическая физика, которой в настоящее время приписывается множество «грехов». Потенциальная энергия U = (–e 0)V ; заряд ядра Ze 0 ; Для кругового движения:
Полная энергия отрицательна. Разрешенные радиусы:

Отметим интересное обстоятельство появления отрицательной энергии электронов в атомах. Это понятие возникло исключительно из-за отрицательного знака заряда электрона, который носит условный характер, определенный человеком. Указанные формулы написаны в системе СГС. Перевод формул в менее запутанную систему СИ дает следующее написание:

где r 1 – радиус первой орбиты в атоме водорода, n = 1, 2, 3, ... – квантовые числа, соответствующие номерам стационарных орбит у водорода.
Везде в формулах оказалась электрическая константа
ξ = 8,98755179·10 9 [m 3 kg ·a –2 s –4 ],
которая есть обратная величина привычной электрической проницаемости вакуума.
Итак, модель атома Бора пришла в противоречие с существовавшей тогда классической физикой.
- Согласно классике, электрон, двигающийся с центростремительным ускорением, обязан излучать электромагнитную энергию.
- В атоме существуют стационарные круговые орбиты, на которых не происходит излучение электронов, и они не падают на ядро в результате расхода энергии.
Сделан вывод, что рожденная таким образом квантовая механика противоречит классической физике в микро мире. Сложилась странная ситуация, в результате которой появился барьер в физике, изучающей единую и неделимую природу. Квантовая механика находит правила устройства микромира и не отвечает на такие вопросы, – что мешает излучению электронов, находящихся на стационарных орбитах? Излучение или поглощение электромагнитных волн электронами в атомах происходит только при их переходах между стационарными орбитами.
Посмотрим, что дает среда существования вещества классической физике и квантовой механике – физический вакуум, имеющий электрическую структуру, погруженную в магнитный (массовый) континуум. В основных чертах эта среда отвечает механической модели, использованной гениальным Максвеллом при выводе своих формул, безотказно работающих до сего времени. Важным элементом понимания сущности инерции является ее возникновение как сопротивление дипольной среды ускоренному движению:
f = b Δr a ~ ma ,
где b = ξ (e 0 2 / Δr rb r e 2) = 1,155406·10 19 [kg ·s –2 ] – электрическая упругость диполя структуры вакуума, r a – деформация диполя структуры под действием силы инерции тела массы m и ускорения а . Знак пропорциональности «~» использован из понимания того, что тело взаимодействует не с одним диполем структуры, а с некоторым кластером или доменом структуры вакуума. Для того, чтобы устранить кажущееся противоречие между классической физиков и КМ, необходим логический вывод: на стационарных орбитах электроны движутся без инерции . Нет центробежной и нет центростремительной сил, создающих классическое ускорение. Существуют такие орбиты или пути движения частиц (электронов) в структуре вакуума, которые не обладают сопротивлением ускоренному движению. В этом отношении круговое движение электронов, обладающих зарядом (электрической напряженностью) и собственным магнитным моментом, а также магнитным моментом вращательного движения, подобно вращению генератора Рощина – Година , в котором все указанные элементы существуют. На опыте генератора происходило уменьшение инерции и веса ротора.
Перейдем к параметрам вакуума. Наиболее важным является то, что константа Планка полностью определяется основными параметрами структуры среды:
h = 2π e 0 2 α –1 √(ξ / η) [J ·s ].
Здесь появилась магнитная константа вакуума
η = 1·10 7 [m –1 kg ·a 2 s 2 ]
как обратная величина магнитной проницаемости и постоянная тонкой структуры
α –1 = 137,035999.
Подстановка h в формулу для первой орбиты водорода дает:
r 1 = (1/η)·(e 0 2 α –2 / m e ).
Орбита зависит от элементарного заряда структуры среды, ее магнитной константы и наиболее фундаментальной величины нашей Вселенной – постоянной тонкой структуры. Массу электрона можно заменить на другие параметры среды:
m e = (1/η)·[e 0 2 / 2(r e + Δr rb )];
в результате получим, что:
r 1 = 2α –2 (r e + Δr rb ) = 5,29177245·10 –11 [m ].
Радиус первой орбиты определяется только величиной постоянной тонкой структуры и основными метрическими характеристиками среды. Очевидно, совпадение R e = 2(r e + Δr rb ), однако могут быть отклонения величины Δr от Δr rb , так как их полная идентичность не установлена. Выше было дано замечание о совпадении классического радиуса с выводами из равенства энергий фотона и электрона – позитрона.
При каких условиях сопротивление среды ускорению равно нулю? Возможно только одно: в условии инерции f = b Δr a ~ ma отсутствует ускорение и Δr a = 0. Это означает, что движение частиц вообще и электрона в частности может происходить так, что частица не взаимодействует с решеткой вакуума, двигаясь строго по существующему точному кругу или сфере зарядов одного знака (для электрона «–»). При этом нет ни гравитации, ни инерции. Гравитация и инерция возникают только при движении частиц и макро тел с пересечением электронной структуры вакуума. Для частиц, двигающихся от заряда к заряду одинакового знака, в общем случае характерна криволинейная траектория в отличие от движения частиц по избранным круговым траекториям. Круговые траектории располагаются на сфере, проходящей через заряды диполей одного знака. Задача нахождения сфер в решетке вакуума разрешима на основе обычной геометрии в пространстве. Криволинейные пути частиц ассоциируются с волнами Де Бройля λ = h / mV и наиболее простой формой траектории будет винтообразное движение с малой амплитудой.
Из курса физики вы знаете, что атом любого вещества состоит из ядра и обращающихся вокруг него электронов. Такую модель атома предложил выдающийся английский физик Э. Резерфорд. Основываясь на этой модели, один из основоположников квантовой механики датский физик Н. Бор в 1913 году произвел первые правильные расчеты атома водорода, достаточно хорошо совпавшие с экспериментальными данными. Теория атома водорода, предложенная Бором, сыграла чрезвычайно важную роль в развитии квантовой механики, хотя в дальнейшем и претерпела существенные изменения.
Атом водорода. Постулаты Бора . Согласно модели Резерфорда-Бора атом водорода состоит из однократно заряженного положительного ядра и одного электрона, обращающегося вокруг него. В первом приближении можно предположить, что движение электрона происходит по траектории, представляющей собой окружность, в центре которой находится неподвижное ядро. В соответствии с требованиями классической электродинамики всякое ускоренное движение заряженного тела (в том числе и электрона) должно сопровождаться испусканием электромагнитных волн. В рассматриваемой модели атома электрон движется с колоссальным центростремительным ускорением, и поэтому он должен был бы непрерывно испускать свет. При этом энергия его должна была бы уменьшаться, а сам электрон должен был бы все ближе и ближе смещаться к ядру. Закончилось бы это тем, что электрон объединился бы с ядром ("упал" бы на ядро). Однако ничего подобного не происходит и атомы в невозбужденном состоянии не испускают света. Для объяснения этого факта Бор предложил два основных постулата.
Согласно первому постулату Бора электрон может находиться только на таких орбитах, для которых момент количества движения электрона (то есть произведение количества движения электрона mν на радиус орбиты ) кратен значению (где - постоянная Планка) * . Пока электрон находится на одной из таких орбит, излучения энергии не происходит. Каждой разрешенной орбите электрона соответствует определенная энергия, или определенное энергетическое состояние атома, называемое стационарным. Находясь в стационарном состоянии, атом не излучает света. Математически первый постулат Бора можно записать так:

где ![]() - некоторое целое число, называемое главным квантовым числом.
- некоторое целое число, называемое главным квантовым числом.
* (Постоянная Планка является универсальной физической константой и имеет смысл произведения энергии на время, называемого в механике действием. Благодаря тому что величина h представляется как бы элементарным количеством действия, постоянная Планка называется квантом (порцией) действия. Введение в физику понятия кванта действия было началом создания важнейшей физической теории XX века - квантовой теории. Квант действия очень мал: )
Второй постулат Бора содержит утверждение, что поглощение или испускание света атомом происходит только при переходах атома из одного стационарного состояния в другое. При этом энергия поглощается или испускается определенными порциями, квантами, значение которых hν определяется разностью энергий, соответствующих начальному и конечному стационарным состояниям атома:
![]()
где - энергия начального состояния атома, - энергия его конечного состояния, ν - частота света, испущенного или поглощенного атомом. Если ![]() то энергия излучается атомом, если же
то энергия излучается атомом, если же ![]() то поглощается.
то поглощается.
Позже кванты света получили название фотонов .
Таким образом, по теории Бора электрон в атоме не может изменять свою траекторию постепенно (непрерывно), а может лишь "перепрыгивать" с одной стационарной орбиты на другую. При переходе со стационарной орбиты, более удаленной от ядра, на стационарную орбиту, расположенную ближе к ядру, как раз и происходит испускание света.
Радиусы орбит и энергетические уровни атомов . Радиусы разрешенных электронных орбит можно найти, используя закон Кулона, соотношения классической механики и первый постулат Бора. Их значения определяются выражением
![]()
Самой близкой к ядру разрешенной орбите соответствует n = 1. Используя полученные экспериментально значения величин m, e и A, находим для ее радиуса значение
Эта величина как раз и принимается за радиус атома водорода. Любая другая орбита с квантовым числом n имеет радиус
![]()
Таким образом, радиусы последовательно расположенных электронных орбит возрастают как квадрат числа n (рис. 1).

Значение полной энергии атома, соответствующей нахождению электрона на n-ой орбите, определяется формулой

Эти значения энергий называются энергетическими уровнями атома, Если по вертикальной оси откладывать возможные значения энергии атома, то можно получить так называемый энергетический спектр разрешенных состояний атома (рис. 2).

Расстояние между последовательно расположенными энергетическими уровнями быстро уменьшается. Это можно легко объяснить: увеличение энергии атома (за счет поглощения атомом энергии извне) сопровождается переходом электрона на все более удаленные орбиты, где взаимодействие между ядром и электроном становится более слабым. По этой причине переход между соседними удаленными орбитами связан с очень малым изменением энергии. Энергетические уровни при этом располагаются настолько близко, что спектр становится практически непрерывным. В верхней части непрерывный спектр заканчивается уровнем ионизации атома (n = ∞), соответствующим полному отделению электрона от ядра (электрон становится свободным).
Знак "-" в выражении для полной энергии атома указывает на то, что энергия атома тем меньше, чем ближе к ядру находится электрон. Для того чтобы удалить электрон от ядра, необходимо затратить определенную энергию, то есть сообщить атому некоторую энергию извне. Энергия атома принимается равной нулю при n = ∞, т. е. в случае, когда атом ионизирован. Именно поэтому значениям соответствуют отрицательные значения энергии. Уровню с n = 1 соответствуют минимальная энергия атома и минимальный радиус разрешенной орбиты электрона. Этот уровень называется основным или невозбужденным. Уровни с n = 2, 3, 4, ... называются уровнями возбуждения.
Квантовые числа . В теории Бора предполагалось, что электронные орбиты имеют вид окружностей. Эта теория дала достаточно хорошие результаты только при рассмотрении самого простого атома - атома водорода. Но уже при расчете атома гелия она не смогла дать количественно правильные результаты. Определенным шагом вперед была планетарная модель атома, предполагавшая движение электронов подобно планетам солнечной системы по эллиптическим орбитам, в одном из фокусов которых располагалось ядро. Однако и эта модель быстро исчерпала себя, не дав ответа на многие вопросы.
Это связано с принципиальной невозможностью определения характера движения электрона в атоме. В доступном нашему наблюдению макромире нет аналогов этого движения. Мы не можем не только проследить путь движения электрона, но и даже определить точно его местонахождение в какой-либо определенный момент времени. Само понятие орбиты, или траектории движения электрона в атоме, лишено физического смысла. Никакой определенной последовательности появления электрона в различных точках пространства установить нельзя, он оказывается как бы "размазанным" в некоторой области, называемой обычно электронным облаком. Облако это, например, для невозбужденного атома водорода имеет форму шара, но плотность его не одинакова. Вероятность обнаружения электрона будет наибольшей вблизи сферы с радиусом r 1 , соответствующим радиусу первой боровской орбиты. В дальнейшем под орбитой электрона в атоме мы будем понимать геометрическое место точек, которые характеризуются наибольшей вероятностью обнаружения электрона, или, другими словами, область пространства с наибольшей плотностью электронного облака.
Всегда сферическим электронное облако будет лишь для случая невозбужденного состояния атома водорода, когда главное квантовое число n = 1 (рис. 3, а). Если же n = 2, то, помимо сферического облака, размеры которого будут теперь в четыре раза больше, электрон может создать облако в виде своеобразной гантельки (рис. 3, б). С появлением несферичности области преимущественной локализации электрона (электронного облака) связано введение второго квантового числа l, называемого орбитальным квантовым числом . Каждому значению главного квантового числа n соответствуют положительные целочисленные значения квантового числа l от нуля до (n - 1):

Так, если n = 1, то l имеет единственное значение, равное нулю. Если же n = 3, то l может принимать значения 0, 1, 2. При n = 1 имеется только сферическая орбита, поэтому и l = 0. Когда n = 2, возможны как сферическая, так и гантелеобразные орбиты, поэтому и l может быть равным либо нулю, либо единице.
Если n = 3, то l = 0, 1, 2. Электронное облако, соответствующее значению l = 2, приобретает уже довольно сложный характер. Для нас, однако, важна не форма электронного облака, а то, какая ему соответствует энергия атома.
Энергия атома водорода определяется только значением главного квантового числа n и не зависит от значения орбитального числа l. Иначе говоря, если n = 3, то атом будет иметь определенную энергию W 3 независимо от того, на какой из возможных орбит, соответствующих данному значению n и различным возможным значениям l, находится электрон. Это означает, что при возвращении с уровня возбуждения на основной уровень атом будет испускать фотоны, энергия которых не зависит от значения l.
Рассматривая пространственную модель атома, необходимо иметь в виду, что электронные облака в нем имеют строго определенную ориентацию. Положение электронного облака в пространстве относительно выбранного каким-либо образом направления задается магнитным квантовым числом m, которое может принимать целочисленные значения от -l до +l, включая 0. При данной форме (данном значении l) электронное облако может иметь несколько различных ориентаций в пространстве. При l = 1 их будет три, соответствующих значениям магнитного квантового числа т, равным -1, 0 и +1. Если l = 2, то различных ориентаций электронного облака будет 5, соответствующих значениям m = -2, -1, 0, +1 и +2. Естественно, что если уж форма электронного облака в свободном атоме водорода не влияет на энергию атома, то тем более не влияет на энергию атома ориентация этого облака в пространстве.
Наконец, при более детальном рассмотрении экспериментальных данных выяснилось, что сами электроны могут находиться на орбитах в двух возможных состояниях, определяемых направлением так называемого спина электрона .
Но что такое спин электрона?
В 1925 году английские физики Дж. Уленбек и С. Гоудсмит для объяснения тонкой структуры линий в оптических спектрах некоторых элементов предложили гипотезу, согласно которой каждый электрон вращается вокруг своей собственной оси подобно волчку или веретену. При таком вращении электрон приобретает некоторый момент импульса, который и получил название спина (в переводе с английского спин означает вращение, веретено). Поскольку вращение может происходить по часовой стрелке или против, то и спин (иначе говоря, вектор момента импульса) может иметь два направления. В единицах спин равен 1 / 2 , а благодаря различным направлениям имеет знак "+" или "-". Таким образом, ориентация электрона на орбите определяется спиновым квантовым числом о, равным ± 1 / 2 . Отметим, что и ориентация спина, как и ориентация орбиты электрона, не влияет на энергию атома водорода, находящегося в свободном состоянии.
Более поздние исследования и расчеты показали, что объяснить спин электрона простым вращением его вокруг оси нельзя. При подсчете угловой скорости вращения электрона для объяснения экспериментальных данных выяснилось, что линейная скорость точек, лежащих на экваторе электрона (в предположении, что электрон имеет шарообразную форму), должна быть больше скорости света, чего не может быть. Спин является некоторой неотъемлемой характеристикой электрона, такой, например, как его масса или заряд.
Квантовые числа - адрес электрона в атоме . Итак, мы выяснили, что для описания движения электрона в атоме, или, как говорят физики, для определения состояния электрона в атоме, необходимо задать набор из четырех квантовых чисел: n, l, m и σ.
Главное квантовое число n определяет, грубо говоря, размеры электронной орбиты. Чем больше n, тем большее пространство охватывает соответствующее электронное облако. Задаваясь значением n, мы тем самым определяем номер электронной оболочки атома. Само число n может принимать любые целочисленные значения от 1 до ∞:
Орбитальное квантовое число l определяет форму электронного облака. Из всей совокупности орбит, относящихся к одному и тому же значению n, орбитальное число l выделяет орбиты, имеющие одинаковую форму. Каждому значению l соответствует своя подоболочка. Число подоболочек равно n, так как l может принимать значения от 0 до (n - 1):
Магнитное квантовое число m определяет пространственную ориентацию орбиты в группе орбит, имеющих одинаковую форму, то есть относящихся к одной подоболочке. В каждой подоболочке насчитывается (2l + 1) различно ориентированных орбит, поскольку m может принимать значения от 0 до ±l:
Наконец, спиновое квантовое число а определяет ориентацию спина электрона на заданной орбите. Значений у σ всего два:

Рассматривая атом водорода и оперируя понятиями "оболочка", "подоболочка", "орбита", мы говорили не столько о строении атома, сколько о возможностях, открывающихся перед единственным электроном, содержащимся в этом атоме. Электрон в атоме водорода может переходить с оболочки на оболочку и с орбиты на орбиту в пределах одной оболочки.
Гораздо сложнее оказывается картина распределения электронов и возможностей их переходов в многоэлектронных атомах.
Вернемся в 1911 год. К этому времени дискретность микромира проявилась наиболее ярко в атомных спектрах. Оказалось, что атомы поглощают и испускают свет только определенной длины волны, причем спектральные линии группируются в так называемые серии (рис. 3.1).
Рис. 3.1. Длины волн, излучаемые атомом водорода: спектр состоит из серий (показаны три первые)
-
последовательностей линий, сгущающихся к некоторому (своему для каждой серии) предельному минимальному
значению ; только четыре линии серии Бальмера лежат в видимом диапазоне

Рис. 3.2. (a) Линейчатые спектры излучения газообразных водорода, ртути и гелия: (b) спектр поглощения водорода

Рис. 3.3. Непрерывные спектры излучения дают нагретые твёрдые и жидкие вещества, сильно сжатые газы, высокотемпературная плазма
Для спектра водорода, простейшего из атомов, была установлена (не выведена, а угадана!) несложная формула
|
|
Здесь -
длина волны излучения атома водорода, n
и k > n
-
целые числа, R
-
так называемая постоянная Ридберга
(![]() , где -
внесистемная единица энергии «Ридберг», равная половине атомной единице энергии).
Оказалось, что серия Лаймана описывается этой формулой при значениях ,
серия Бальмера -
при , серия Пашена -
при и т. д. Предельные (минимальные) значения для длин волн получаются из (3.1) при :
, где -
внесистемная единица энергии «Ридберг», равная половине атомной единице энергии).
Оказалось, что серия Лаймана описывается этой формулой при значениях ,
серия Бальмера -
при , серия Пашена -
при и т. д. Предельные (минимальные) значения для длин волн получаются из (3.1) при :
![]()

Рис. 3.4. Йоханнес Роберт Ридберг (1854–1919)

Рис. 3.5. Теодор Лайман (1874–1954)

Рис. 3.6. Спектральная серия Лаймана

Рис. 3.7. Иоганн Якоб Бальмер (1825–1898)
Рис. 3.8. Видимые линии излучения водорода в серии Бальмера. Hα - красная линия справа, имеющая длину волны 656,3 нм. Самая левая линия - Hε, соответствует излучению уже в ультрафиолетовой области спектра на длине волны 397,0 нм

Рис. 3.9. Луис Карл Генрих Фридрих Пашен (1865–1947)
Рис. 3.10. Все линии серии Пашена расположены в инфракрасном диапазоне
Кроме того, в результате изучения свойств газов к тому времени было известно, что размеры атомов приблизительно
равны . Поэтому теория, объясняющая спектр и размеры атомов, должна была включать в себя какой-то параметр, позволяющий построить величину с размерностью длины (постоянных e
и m
-
заряда и массы электрона -
для этого недостаточно). Такого параметра в классической теории не было. Им могла бы стать постоянная Ридберга, но ее происхождение было темно и загадочно.
В 1911 году Э. Резерфорд опубликовал теоретическую работу (Rutherford E., Philosophical Magazine, v. 21, p. 669–688 , 1911), в которой на базе анализа экспериментов, выполненных в 1908–1909 годах его учениками - стажером Гансом Гейгером и аспирантом Эрнстом Марсденом - (Geiger H., Marsden T., Proceedings of the Royal Society of London, Series A, v. 82, p. 495–499 , 1909) утверждал наличие внутри атома положительно заряженного ядра, в котором сосредоточена практически вся масса атома.

Рис. 3.11. Эрне́ст Ре́зерфорд (1871–1937)
Видео 3.2. Немного истории. Черная шляпа и модель рассеяния.В последствии, в одной из своих лекций сам Э. Резерфорд вспоминал о тех временах следующим образом (цитируется по книге Дж. Тригг, Решающие эксперименты в современной физике, Москва, «МИР», 1974, стр. 77): «…Я помню… ко мне пришел очень взволнованный Гейгер и сказал: «Мы, кажется, получили несколько случаев рассеяния - частиц назад…». Это самое невероятное событие, которое было в моей жизни. Это почти также невероятно, как если бы вы выстрелили 15-дюймовым снарядом в папиросную бумагу и он, отразившись от неё, попал бы в вас. При анализе этого я понял, что такое рассеяние назад должно быть результатом однократного столкновения и, проведя расчеты, увидел, что это никоим образом невозможно, если не предположить, что подавляющая часть массы атома сконцентрирована в крошечном ядре. Именно тогда у меня и зародилась идея об атоме с крошечным массивным центром, в котором сосредоточен заряд». От себя добавим, что слова «рассеяние назад» фактически означали рассеяние на 150 градусов, рассеяние на большие углы не позволяла наблюдать конструкция использованной в тот момент установки.
Принципиальная схема опытов Резерфорда представлена на рис. 3.12. Схему реальной установки можно найти в цитированной выше книге Дж. Тригга.

Рис. 3.12. Схема опыта Резерфорда по рассеянию - частиц
Видео 3.3. Натурный опыт Резерфорда на лабораторной установке. Видео 3.4. Опыт Резерфорда «изнутри» (лабораторная установка). Видео 3.5. Компьютерная модель опыта Резерфорда.От радиоактивного источника, заключенного в свинцовый контейнер, частицы направлялись на тонкую фольгу Ф из исследуемого металла. Рассеянные частицы попадали на экран, покрытый слоем кристаллов сульфида цинка, способных светиться под ударами быстрых заряженных частиц. Сцинтилляции (вспышки) на экране наблюдались глазом с помощью микроскопа. Наблюдения рассеянных частиц в опыте Резерфорда можно было проводить под различными углами к первоначальному направлению пучка. Было обнаружено, что большинство частиц проходит через тонкий слой металла, практически не испытывая отклонения. Однако небольшая часть частиц отклоняется на значительные углы, превышающие 30° . Очень редкие частицы (приблизительно одна на десять тысяч) испытывали отклонение на углы, близкие к . Очевидно, что частица может быть отброшена назад, только если положительный заряд атома и его масса сосредоточены в очень малом объеме внутри атома. Таким образом, было открыто атомное ядро - тело малых по сравнению с атомом размеров, в котором сосредоточен весь положительный заряд и практически вся его масса. Размеры ядра были оценены Э. Резерфордом в работе 1911 года, оценка дала меньше или порядка .
Видео 3.6. Прицельный параметр и форма траектории. Видео 3.7. Заряд рассеиваемой частицы и форма траектории. Видео 3.8. Энергия рассеиваемой частицы и форма траектории. Видео 3.9. Заряд ядра и форма траектории.
Рис. 3.13. Схема рассеяния альфа-частиц на ядре атома золота

Рис. 3.14. Схема рассеяния потока альфа-частиц в тонкой золотой фольге
Возникла планетарная модель атома водорода: протон с электроном на орбите. Физики любят единые модели, а здесь так красиво в малом повторялось большое, в атоме - Солнечная система.

Рис. 3.15. Схема ядерной (планетарной) модели атома Резерфорда
Проблема состояла в том, что электрон, совершающий финитное, а следовательно - ускоренное движение около ядра, должен упасть на ядро. Дело в том, что электрон заряжен и при ускоренном движении должен испускать электромагнитное излучение, то есть стационарное движение невозможно. Классическая электродинамика предсказывает, что, быстро потеряв свою энергию и момент импульса орбитального движения, электрон должен упасть на ядро примерно за . Свет за это время проходит около 1.5 см (получается, что мы видим лишь «мертвые» атомы, но это не так!). Резерфорд понимал проблему, но сознательно концентрировался на факте существования ядра, полагая, что вопрос об устойчивости атома будет решен при исследовании поведения атомных электронов. Это суждено было сделать в 1913 г. Н. Бору , предложившему новую теорию атома.


Рис. 3.16. Неустойчивость модели атома Резерфорда
Постулаты Бора
Первый постулат Бора
Здесь прослеживается «насильственное» введение дискретности (разрешены не все орбиты), а также типичное для физики «заметание проблемы под ковер»: если чему-то не находится объяснений, принимают это как данность и изучают следствия в надежде, что когда-нибудь поймут и причину.

Рис. 3.17. Иллюстрация первому постулату Бора
Второй постулат Бора
Этот постулат отражает сохранение энергии и соотношение Планка – Эйнштейна .

Рис. 3.18. Иллюстрация ко второму постулату Бора
Третий постулат Бора
Неизбежное следствие: так как остальные орбиты для электрона запрещены, переход осуществляется скачком; о пути и энергии электрона между орбитами говорить не имеет смысла: законы механики там не применимы.
Четвертый постулат Бора
Постоянная Планка ħ имеет размерность момента количества движения и вместе с зарядом электрона е и его массой m позволяет образовать параметр размерности длины. Это приводит к возможности вычислить размеры атома.

Рис. 3.19. Нильс Хе́нрик Дави́д Бор (1885–1962)
Применение постулатов Бора
Классическая механика для электрона, вращающегося по круговой орбите радиусом R со скоростью v вокруг ядра с зарядом Ze , дает уравнение движения


Поэтому энергия Е и момент импульса L электрона выражаются через радиус орбиты R :

Если к последнему выражению применение условие квантования Бора L=nħ (n=1, 2, 3, … ), то получатся следующие результаты.

Рис. 3.20. Модель атома Бора
Характеристики водородоподобного атома
Радиусы разрешенных орбит
|
|
Энергия электрона на стационарной орбите
Константа а
В
,
имеющая размерность длины, называется радиусом Бора: ![]() . Смысл числа -
номер разрешенной орбиты. Радиус Бора -
радиус низшей орбиты в атоме водорода .
. Смысл числа -
номер разрешенной орбиты. Радиус Бора -
радиус низшей орбиты в атоме водорода .
Формула (3.3) определяет дискретные значения энергии, которые может иметь электрон в атоме водорода, или, как говорят, энергетические уровни. Отрицательные значения соответствуют связанным состояниям электрона в атоме, то есть движениям в ограниченной области пространства (аналог в классической физике - движение планет по эллипсам в отличие от гиперболических и параболических траекторий, уходящих на бесконечность).
При решении задач о поведении электрона в атоме обычно возникают выражения, включающие квадрат электрического заряда электрона в комбинации с электрической постоянной . Весьма полезно ввести безразмерную комбинацию фундаментальных мировых постоянных - так называемую постоянную тонкой структуры :
|
|
которая, совместно с атомным номером и номером орбиты , определяет масштаб релятивистских эффектов в атоме. Для того, чтобы это было лучше видно, перепишем формулу (3.3) так, чтобы в её правую часть входила постоянная тонкой структуры:
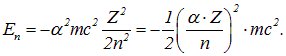
Из-за множителя характерные для атома энергии оказываются на четыре порядка меньше энергии покоя электрона. Это проявление нерелятивизма достаточно легких атомных систем. Как видно из последнего выражения в приведенной выше формуле, релятивистские эффекты перестают быть малыми поправками для ближних к ядру электронов в тяжелых атомах.
Пример 1. Определим скорость электрона на n -й орбите атома Бора. Радиус n-й орбиты определяется формулой
где а В - радиус Бора. Скорость электрона v можно выразить через момент импульса L=nħ:

Выражение для радиуса Бора упростим, используя введенную постоянную тонкой структуры:
|
|
Подставляя это выражение в полученную выше формулу для скорости электрона, получаем для n -й орбиты
Рис. 3.21. Схема энергетических уровней и переходов в атоме водорода по теории Бора:
сплошные линии (переходы сверху вниз) - излучение, пунктирные линии (переходы снизу вверх) - поглощение.
Показаны границы (пределы) серий ![]() , которым соответствуют переходы с уровня с
, которым соответствуют переходы с уровня с
- границы между континуумом и дискретным спектром
Экспериментальное подтверждение утверждение Бора о дискретности энергетического спектра атомов нашло в опытах Франка - Герца, которые заключались в бомбардировке паров ртути электронами в вакуумной трубке и измерении зависимости анодного тока от ускоряющей разности потенциалов. Схема опыта приведена на рис. 3.22.

Рис. 3.22. Схема опыта Франка - Герца
В трубке, заполненной парами ртути под небольшим давлением (около 1 мм. рт. ст.), имеются три электрода: анод, катод и сетка. Электроны, вылетающие с поверхности подогретого катода вследствие термоэлектронной эмиссии, ускоряются напряжением U , приложенным между катодом и сеткой. Это напряжение можно менять с помощью потенциометра П . Между анодом и сеткой приложено слабое обратное поле с разностью потенциалов порядка 0,5ВВ , тормозящее движение электронов к аноду. Определялась зависимость тока I в цепи анода от приложенного напряжения U . Полученные результаты приведены на рис. 3.23.

Рис. 3.23. Зависимость тока I в цепи анода от приложенного напряжения U в опыте Франка - Герца
Сила тока сначала монотонно возрастает, достигает максимума при напряжении 4,9 В , после чего с ростом U резко падает, достигает минимума и снова начинает расти. Максимумы силы тока повторяются при напряжениях 9,8 В , 14,7 В и т. д. Чередование максимумов на равном расстоянии друг от друга доказало дискретность изменения энергии атома.
Видео 3.10. Опыт Франка и Герца. Демонстрационная установка. Видео 3.11. Опыт Франка и Герца. Сравнение ВАХ для неона и гелия. Видео 3.12. Опыт Франка и Герца. Лабораторная установка 1. Видео 3.12. Опыт Франка и Герца. Лабораторная установка 2.
Атомный номер элемента - целое число, так что после округления получаем Z = 2 , что соответствует гелию.
Как отмечалось выше, еще до появления теории Бора был изучен спектр водородного атома и эмпирически установлена формула (3.1). Но при наблюдении спектра Солнца были замечены линии, казалось бы, нарушающие эту формулу, так как они соответствовали полуцелым значениям n и k . После появления теории Бора стало ясно, что квантовые числа n и k все-таки должны быть целыми, а кажущиеся полуцелые значения можно объяснить по-другому. Действительно, из формулы (3.6) для частот, испускаемых водородоподобным атомом,следует, что

то есть наблюдавшиеся линии принадлежат иону элемента с Z = 2 . Как известно, этот элемент носит «солнечное» имя - гелий.
Чтобы получить согласие с результатами наблюдений, Бор предположил, что электрон в атоме водорода движется только по тем круговым орбитам, для которых его момент импульса
где n - квантовые числа, т – масса электрона, - его скорость, r - радиус орбиты. (Рассуждения, которые привели Бора к этому предположению мы опустим.)
С помощью этого правила квантования можно найти радиусы круговых стационарных орбит водорода и водородоподобных систем: ионов атомов с одним оставшимся электроном (Н, Не + , Li + + , …) и соответствующие им энергии. Пусть заряд ядра водородоподобной системы равен e . Масса ядра значительно больше массы электрона, поэтому ядро при движении электрона можно считать неподвижным. Следуя Бору, будем предполагать, что электрон движется вокруг ядра по окружности радиуса r .
Согласно 2-му закону Ньютона
 (3.12.9)
(3.12.9)
Решая совместно (3.12.8) и (3.12.9), можно найти радиусы электронных орбит и их скорости на этих орбитах:
![]() . (3.12.10)
. (3.12.10)
Таким образом, радиус первой (ближайшей к ядру) орбиты электрона в атоме водорода (его обозначают обычно и называют первым Боровским радиусом )
![]() нм (3.12.11)
нм (3.12.11)
Внутренняя энергия атома складывается из кинетической энергии электрона (ядро полагают неподвижным) и потенциальной энергии взаимодействия электрона с ядром. С учетом (3.12.10) получим:
 . (3.12.12)
. (3.12.12)
При переходе атома водорода (Z =1) из состояния в состояние излучается фотон
 . (3.12.13)
. (3.12.13)
Тогда частота испущенного света равна
 , (3.12.14)
, (3.12.14)
Что соответствует обобщенной формуле Бальмера, если постоянная Ридберга определяется . (3.12.15)
Расчет по этой формуле хорошо согласуется с экспериментально определенным значением.
Схема энергетических уровней (разрешенных значений энергии) атома водорода приведена на рис.3.12.4. Там же показаны возможные переходы, сопровождающиеся излучением фотонов определенной частоты.

Лекция 3.13.
Волновые свойства частиц вещества.
Гипотеза де-Бройля. Волны де-Бройля.
Как было сказано ранее, свет (и вообще излучение) имеет двойственную природу: в одних явлениях (интерференция, дифракция и др.) свет проявляет себя как волны, в других явлениях с не меньшей убедительностью – как частицы. Это и побудило де-Бройля (в 1923 г.) высказать идею о том, что материальные частицы должны обладать и волновыми свойствами, т.е. распространить подобный корпускулярно-волновой дуализм на частицы с массой покоя, отличной от нуля.
Если с такой частицей связана какая-то волна, можно ожидать, что она распространяется в направлении скорости υ частицы. О природе этой волны ничего определенного де-Бройлем не было высказало. Не будем и мы пока выяснять их природу, хотя сразу же подчеркнем, что эти волны не электромагнитные. Они имеют, как мы увидим далее, специфическую природу, для которой нет аналога в классической физике.
Итак, де-Бройль высказал гипотезу, что соотношение для импульса p=ћω/c , относящееся к фотонам, имеет универсальный характер, т. е. частицам можно сопоставить волну, длина которой
Эта формула получила название формулы де-Бройля , а λ – дебройлевской длины волны частицы с импульсом р .
Де-Бройль также предположил, что пучок частиц, падающих на двойную щель, должен за ними интерферировать.
Вторым, независимым от формулы (3.13.1), соотношением является связь между энергией Е частицы и частотой ω дебройлевской волны:
В принципе энергия Е определена всегда с точностью до прибавления произвольной постоянной (в отличие от ΔЕ ), следовательно, частота ω является принципиально ненаблюдаемой величиной (в отличие от дебройлевской длины волны).
С частотой ω и волновым числом k связаны две скорости - фазовая υ ф и групповая u :
![]() (3.13.3)
(3.13.3)
Умножив числитель и знаменатель обоих выражений на ћ с учетом (3.13.1) и (3.13.2), получим, ограничившись рассмотрением только нерелятивистского случая, т.е. полагая E = p 2 /2m (кинетическая энергия):
![]() (3.13.4)
(3.13.4)
Отсюда видно, что групповая скорость равна скорости частицы, т. е. является принципиально наблюдаемой величиной, в отличие от υ ф ‑ из-за неоднозначности Е .
Из первой формулы (3.13.4) следует, что фазовая скорость дебройлевских волн
 (3.13.5)
(3.13.5)
т. е. зависит от частоты ω, а значит дебройлевские волны обладают дисперсией даже в вакууме. Далее будет показано, что в соответствии с современной физической интерпретацией фазовая скорость дебройлевских волн имеет чисто символическое значение, поскольку эта интерпретация относит их к числу принципиально ненаблюдаемых величин. Впрочем, сказанное видно и сразу, так как Е в (3.13.5) определена, как уже говорилось, с точностью до прибавления произвольной постоянной.
Установление того факта, что согласно (3.13.4) групповая скорость дебройлевских волн равна скорости частицы, сыграло в свое время важную роль в развитии принципиальных основ квантовой физики, и в первую очередь в физической интерпретации дебройлевских волн. Сначала была сделана попытка рассматривать частицы как волновые пакеты весьма малой протяженности и таким образом решить парадокс двойственности свойств частиц. Однако подобная интерпретация оказалась ошибочной, так как все составляющие пакет гармонические волны распространяются с разными фазовыми скоростями. При наличии большой дисперсии, свойственной дебройлевским волнам даже в вакууме, волновой пакет «расплывается». Для частиц с массой порядка массы электрона пакет расплывается практически мгновенно, в то время как частица является стабильным образованием.
Таким образом, представление частицы в виде волнового пакета оказалось несостоятельным. Проблема двойственности свойств частиц требовала иного подхода к своему решению.
Вернемся к гипотезе де-Бройля. Выясним, в каких явлениях могут проявиться волновые свойства частиц, если они, эти свойства, действительно существуют. Мы знаем, что независимо от физической природы волн - это интерференция и дифракция. Непосредственно наблюдаемой величиной в них является длина волны. Во всех случаях дебройлевская длина волны определяется формулой (3.13.1). Проведем с помощью нее некоторые оценки.
Прежде всего, убедимся, что гипотеза де-Бройля не противоречит понятиям макроскопической физики. Возьмем в качестве макроскопического объекта, например, пылинку, считая, что ее масса m = 1мг и скорость V = 1 мкм/с. Соответствующая ей дебройлевская длина волны
![]() (3.13.6)
(3.13.6)
Т. е. даже у такого небольшого макроскопического объекта как пылинка дебройлевская длина волны оказывается неизмеримо меньше размеров самого объекта. В таких условиях никакие волновые свойства, конечно, проявить себя не могут в условиях доступных измерению размеров.
Иначе обстоит дело, например, у электрона с кинетической энергией K и импульсом . Его дебройлевская длина волны
![]() (3.13.7)
(3.13.7)
где K должно быть измерено в электрон-вольтах (эВ). При K = 150 эВ дебройлевская длина волны электрона равна согласно (3.13.7) λ = 0,1нм. Такой же порядок величины имеет постоянная кристаллической решетки. Поэтому, аналогично тому, как в случае рентгеновских лучей, кристаллическая структура может быть подходящей решеткой для получения дифракции дебройлевских волн электронов. Однако гипотеза де-Бройля представлялась настолько нереальной, что довольно долго не подвергалась экспериментальной проверке.
 Экспериментально гипотеза де-Бройля была подтверждена в опытах Дэвиссона и Джермера (1927г.). Идея их опытов заключалась в следующем. Если пучок электронов обладает волновыми свойствами, то можно ожидать, даже не зная механизма отражения этих волн, что их отражение от кристалла будет иметь такой же интерференционный характер, как у рентгеновских лучей.
Экспериментально гипотеза де-Бройля была подтверждена в опытах Дэвиссона и Джермера (1927г.). Идея их опытов заключалась в следующем. Если пучок электронов обладает волновыми свойствами, то можно ожидать, даже не зная механизма отражения этих волн, что их отражение от кристалла будет иметь такой же интерференционный характер, как у рентгеновских лучей.
В одной серии опытов Дэвиссона и Джермера для обнаружения дифракционных максимумов (если таковые есть) измерялись ускоряющее напряжение электронов и одновременно положение детектора D (счетчика отраженных электронов). В опыте использовался монокристалл никеля (кубической системы), сошлифованный так, как показано на рис.3.13. Если его повернуть вокруг вертикальной оси в Рис.3.13.1
 положение, соответствующее рисунку, то в этом положении
положение, соответствующее рисунку, то в этом положении
сошлифованная поверхность покрыта правильными рядами атомов, перпендикулярными к плоскости падения (плоскости рисунка), расстояние между которыми d = 0,215нм. Детектор перемещали в плоскости падения, меняя угол θ. При угле θ = 50 0 и ускоряющем напряжении V = 54B наблюдался особенно отчётливый максимум отраженных Рис.3.13.2.
электронов, полярная диаграмма которых показала на рис.3.13.2.Этот максимум можно истолковать как интерференционный максимум первого порядка от плоской дифракционной решетки с указанным выше периодом в соответствии с формулой
 что видно из рис.3.13.3. На этом рисунке каждая жирная точка представляет собой проекцию цепочки атомов, расположенных на прямой, перпендикулярной плоскости рисунка. Период d
может быть измерен независимо, например, по дифракции рентгеновских лучей. Рис.3.13.3.
что видно из рис.3.13.3. На этом рисунке каждая жирная точка представляет собой проекцию цепочки атомов, расположенных на прямой, перпендикулярной плоскости рисунка. Период d
может быть измерен независимо, например, по дифракции рентгеновских лучей. Рис.3.13.3.
Вычисленная по формуле (3.13.7) дебройлевская длина волны для V = 54B равна 0,167нм. Соответствующая же длина волны, найденная из формулы (3.13.8), равна 0,165нм. Совпадение настолько хорошее, что полученный результат следует признать убедительным подтверждением гипотезы де-Бройля.
Другими опытами, подтверждающим гипотезу де-Бройля, были опыты Томсона и Тартаковского. В этих опытах пучок электронов пропускался через поликристаллическую фольгу (по методу Дебая при изучении дифракции рентгеновского излучения). Как и в случае рентгеновского излучения, на фотопластинке, расположенной за фольгой, наблюдалась система дифракционных колец. Сходство обеих картин поразительно. Подозрение, что система этих колец порождается не электронами, а вторичным рентгеновским излучением, возникающим в результате падения электронов на фольгу, легко рассеивается, если на пути рассеянных электронов создать магнитное поле (поднести постоянный магнит). Оно не влияет на рентгеновское излучение. Такого рода проверка показала, что интерференционная картина сразу же искажалась. Это однозначно свидетельствует, что мы имеем дело именно с электронами.
Г. Томсон осуществил опыты с быстрыми электронами (десятки кэВ), П.С. Тарковский - со сравнительно медленными электронами (до 1,7 кэВ).
Для успешного наблюдения дифракции волн на кристаллах необходимо, чтобы длина волны этих волн была сравнима с расстояниями между узлами кристаллической решетки. Поэтому для наблюдения дифракции тяжелых частиц необходимо пользоваться частицами с достаточно малыми скоростями. Соответствующие опыты по дифракции нейтронов и молекул при отражении от кристаллов были проделаны и также полностью подтвердили гипотезу де-Бройля в применении и к тяжелым частицам.
Благодаря этому было экспериментально доказано, что волновые свойства являются универсальным свойством всех частиц. Они не обусловлены какими-то особенностями внутреннего строения той или иной частицы, а отражают их общий закон движения.
Описанные выше опыты выполнялись с использованием пучков частиц. Поэтому возникает естественный вопрос: наблюдаемые волновые свойства выражают свойства пучка частиц или отдельных частиц?
Чтобы ответить на этот вопрос, В. Фабрикант, Л. Биберман и Н. Сушкин осуществили в 1949 г. опыты, в которых применялись столь слабые пучки электронов, что каждый электрон проходил через кристалл заведомо поодиночке, и каждый рассеянный электрон регистрировался фотопластинкой. При этом оказалось, что отдельные электроны попадали в различные точки фотопластинки совершенно беспорядочным на первый взгляд образом (рис.3.13.4а ). Между тем при достаточно длительной экспозиции на фотопластинке возникала дифракционная картина (рис.3.13.4б ), абсолютно идентичная картине дифракции от обычного электронного пучка. Так было доказано, что волновыми свойствами обладают и отдельные частицы.
 Таким образом, мы имеем дело с микрообъектами, которые обладают одновременно как корпускулярными, так и волно-
Таким образом, мы имеем дело с микрообъектами, которые обладают одновременно как корпускулярными, так и волно-
выми свойствами. Это позволяет нам в дальнейшем говорить
об электронах, но выводы, к которым мы придем, имеют Рис.3.13.4.
общий смысл и в равной степени применимы к любым частицам.
Парадоксальное поведение микрочастиц.
Рассмотренные в предыдущем параграфе эксперименты вынуждают констатировать, что перед нами один из загадочнейших парадоксов: что означает утверждение «электрон - это одновременно частица и волна »?
Попытаемся разобраться в этом вопросе с помощью мысленного эксперимента, аналогичного опыту Юнга по изучению интерференции света (фотонов) от двух щелей. После прохождения пучка электронов через две щели на экране образуется система максимумов и минимумов, положение которых можно рассчитать по формулам волновой оптики, если каждому электрону сопоставить дебройлевскую волну.
В явлении интерференции от двух щелей таятся сама суть квантовой теории, поэтому уделим этому вопросу особое внимание.
Если мы имеем дело с фотонами, то парадокс (частица - волна) можно устранить, предположив, что фотон в силу своей специфичности расщепляется на две части (на щелях), которые затем интерферируют.
 А электроны? Они ведь никогда не расщепляются - это установлено совершенно достоверно. Электрон может пройти либо через щель 1, либо через щель 2 (рис.3.13.5). Следовательно, распределение их на экране Э должно быть суммой распределений 1 и 2 (рис.3.13.5а
) - оно показано пунктирной кривой. Рис.13.13.5.
А электроны? Они ведь никогда не расщепляются - это установлено совершенно достоверно. Электрон может пройти либо через щель 1, либо через щель 2 (рис.3.13.5). Следовательно, распределение их на экране Э должно быть суммой распределений 1 и 2 (рис.3.13.5а
) - оно показано пунктирной кривой. Рис.13.13.5.
Хотя логика в этих рассуждениях безупречна, такое распределение не осуществляется. Вместо этого мы наблюдаем совершенно иное распределение (рис.3.13.5б ).
Не есть ли это крушение чистой логики и здравого смысла? Ведь все выглядит так, как если бы 100 + 100 = 0 (в точке P). В самом деле, когда открыта или щель 1 или щель 2, то в точку P приходит, скажем, по 100 электронов в секунду, а если открыты обе щели, то ни одного!..
Более того, если сначала открыть щель 1, а потом постепенно открывать щель 2, увеличивая ее ширину, то по здравому смыслу число электронов, приходящих в точку P ежесекундно, должно расти от 100 до 200. В действительности же - от 100 до нуля.
Если подобную процедуру повторить, регистрируя частицы, например, в точке O (см. рис.3.13.5б ), то возникает не менее парадоксальный результат. По мере открывания щели 2 (при открытой щели 1) число частиц в точке O растет не до 200 в секунду, как следовало бы ожидать, а до 400!
Как открывание щели 2 может повлиять на электроны, которые, казалось бы, проходят через щель 1? Т. е. дело обстоит так, что каждый электрон, проходя через какую-то щель, «чувствует» и соседнюю щель, корректируя свое поведение. Или подобно волне проходит сразу через обе щели (!?). Ведь иначе интерференционная картина не может возникнуть. Попытка все же определить, через какую щель проходит тот или иной электрон, приводит к разрушению интерференционной картины, но это уже совсем другой вопрос.
Какой же вывод? Единственный способ «объяснения», этих парадоксальных результатов заключается в создании математического формализма, совместимого с полученными результатами и всегда правильно предсказывающего наблюдаемые явления. Причем, разумеется, этот формализм должен быть внутренне непротиворечивым.
И такой формализм был создан. Он ставит в соответствие каждой частице некоторую комплексную пси-функцию Ψ(r , t ). Формально она обладает свойствами классических волн, поэтому ее часто называют волновой функцией . Поведение свободной равномерно движущейся в определенном направлении частицы описывает плоская волна де-Бройля
Но более подробно об этой функции, ее физическом смысле и уравнении, которое управляет ее поведением в пространстве и времени, речь пойдет в следующей лекции.
Возвращаясь к поведению электронов при прохождении через две щели, мы должны признать: тот факт, что в принципе нельзя ответить на вопрос, через какую щель проходит электрон (не разрушая интерференционной картины), несовместим с представлением о траектории. Таким образом, электронам, вообще говоря, нельзя приписать траектории .
Однако при определенных условиях, а именно когда дебройлевская длина волны микрочастицы становится очень малой и может оказаться много меньше, например, расстояния между щелями или атомных размеров, понятие траектории снова приобретает смысл. Рассмотрим этот вопрос более подробно и сформулируем более корректно условия, при которых можно пользоваться классической теорией.
Принцип неопределенности
В классической физике исчерпывающее описание состояния частицы определяется динамическими параметрами, такими как координаты, импульс, момент импульса, энергия и др. Однако реальное поведение микрочастиц показывает, что существует принципиальный предел точности, с которой подобные переменные могут быть указаны и измерены.
Глубокий анализ причин существования этого предела, который называют принципом неопределенности , провел В. Гейзенберг (1927г.). Количественные соотношения, выражающие этот принцип в конкретных случаях, называют соотношениями неопределенностей .
Своеобразие свойств микрочастиц проявляется в том, что не для всех переменных получаются при измерениях определенные значения. Существуют пары величин, которые не могут быть одновременно определены точно.
Наиболее важными являются два соотношения неопределенностей.
Первое из них ограничивает точности одновременного измерения координат и соответствующих проекций импульса частицы. Для проекции, например, на ось х оно выглядит так:
Второе соотношение устанавливает неопределенность измерения энергии, ΔE , за данный промежуток времени Δt :
Поясним смысл этих двух соотношений. Первое из них утверждает, что если положение частицы, например, по оси х известно с неопределенностью Δx , то в тот же момент проекцию импульса частицы на эту же ось можно измерить только с неопределенностью Δp= ћ /Δx . Заметим, что эти ограничения не касаются одновременного измерения координаты частицы по одной оси и проекции импульса - по другой: величины x и p y , y и p x и т. д. могут иметь одновременно точные значения.
Согласно второму соотношению (3.13.11) для измерения энергии с погрешностью ΔЕ необходимо время, не меньшее, чем Δt =ћ /ΔE . Примером может служить «размытие» энергетических уровней водородоподобных систем (кроме основного состояния). Это связано с тем, что время жизни во всех возбужденных состояниях этих систем порядка 10 -8 с. Размытие же уровней приводит к уширению спектральных линий (естественное уширение), которое действительно наблюдается. Сказанное относится и к любой нестабильной системе. Если время жизни ее до распада порядка τ, то из-за конечности этого времени энергия системы имеет неустранимую неопределенность, не меньшую, чем ΔE≈ ћ /τ.
Укажем еще пары величин, которые не могут быть одновременно точно определены. Это любые две проекции момента импульса частицы. Поэтому не существует состояния, в котором бы все три и даже какие-либо две из трех проекций момента импульса имели определенные значения.
Обсудим более подробно смысл и возможности соотношения Δx ·Δp x ≥ћ . Прежде всего, обратим внимание на то, что оно определяет принципиальный предел неопределенностей Δx и Δp x , с которыми состояние частицы можно характеризовать классически, т.е. координатой x и проекцией импульса p x . Чем точнее x , тем с меньшей точностью, возможно установить p x , и наоборот.
Подчеркнем, что истинный смысл соотношения (3.13.10) отражает тот факт, что в природе объективно не существует состояний частицы с точно определенными значениями обеих переменных, x и p х. Вместе с тем мы вынуждены, поскольку измерения проводятся с помощью макроскопических приборов, приписывать частицам не свойственные им классические переменные. Издержки такого подхода и выражают соотношения неопределенностей.
После того, как выяснилась необходимость описывать поведение частиц волновыми функциями, соотношения неопределенностей возникают естественным образом - как математическое следствие теории.
Считая соотношение неопределенностей (3.13.10) универсальным, оценим, как бы оно сказалось на движении макроскопического тела. Возьмем очень маленький шарик массы m = 1мг. Определим, например, с помощью микроскопа его положение с погрешностью Δx≈ 10 -5 см (она обусловлена разрешающей способностью микроскопа). Тогда неопределенность скорости шарика Δυ = Δp /m≈ (ћ /Δx )/m ~ 10 -19 см/с. Такая величина недоступна никакому измерению, а потому и отступление от классического описания совершенно несущественно. Другими словами, даже для такого маленького (но макроскопического) шарика понятие траектории применимо с высокой степенью точности.
Иначе ведет себя электрон в атоме. Грубая оценка показывает, что неопределенность скорости электрона, движущегося по боровской орбите атома водорода, сравнима с самой скоростью: Δυ ≈ υ. При таком положении представление о движении электрона по классической орбите теряет всякий смысл. И вообще, при движении микрочастиц в очень малых областях пространства понятие траектории оказывается несостоятельным .
Вместе с тем, при определенных условиях движение даже микрочастиц может рассматриваться классически, т. е. как движение по траектории. Так происходит, например, при движении заряженных частиц в электромагнитных полях (в электронно-лучевых трубках, ускорителях и др.). Эти движения можно рассматривать классически, поскольку для них ограничения, обусловленные соотношением неопределенностей, пренебрежимо малы по сравнению с самими величинами (координатами и импульсом).
Опыт со щелью . Соотношение неопределенностей (3.13.10) проявляет себя при любой попытке точного измерения положения или импульса микрочастицы. И каждый раз мы приходим к «неутешительному» результату: уточнение положения частицы приводит к увеличению неопределенности импульса, и наоборот. В качестве иллюстрации такой ситуации рассмотрим следующий пример.
Попытаемся определить координату x свободно движущейся с импульсом p частицы, поставив на ее пути перпендикулярно направлению движения экран со щелью шириной b (рис.3.13.6). До прохождения частицы через щель ее проекция импульса p х имеет точное значение: p x = 0. Это значит, что Δ p x = 0, но
 координата x
частицы является совершенно неопреде ленной согласно (3.13.10): мы не можем сказать, Рис.3.13.6.
координата x
частицы является совершенно неопреде ленной согласно (3.13.10): мы не можем сказать, Рис.3.13.6.
пройдет ли данная частица через щель.
Если частица пройдет сквозь щель, то в плоскости щели координата x будет зарегистрирована с неопределенностью Δx ≈ b . При этом вследствие дифракции с наибольшей вероятностью частица будет двигаться в пределах угла 2θ, где θ - угол, соответствующий первому дифракционному минимуму. Он определяется условием, при котором разность хода волн от обоих краев щели будет равна λ (это доказывается в волновой оптике):
В результате дифракции возникает неопределенность значения p х - проекции импульса, разброс которого
Учитывая, что b ≈ Δх и p = 2πћ /λ., получим из двух предыдущих выражений:
![]()
что согласуется по порядку величины с (3.13.10).
Таким образом, попытка определить координату x частицы, действительно, привела к появлению неопределенности Δp в импульсе частицы.
Анализ многих ситуаций, связанных с измерениями, показывает, что измерения в квантовой области принципиально отличаются от классических измерений. В отличие от последних, в квантовой физике существует естественный предел точности измерений. Он в самой природе квантовых объектов и не может быть преодолен никаким совершенствованием приборов и методов измерений. Соотношение (3.13.10) и устанавливает один из таких пределов. Взаимодействие между микрочастицей и макроскопическим измерительным прибором нельзя сделать сколь угодно малым. Измерение, например координаты частицы, неизбежно приводит к принципиально неустранимому и неконтролируемому искажению состояния микрочастицы, а значит и к неопределенности в значении импульса.
Некоторые выводы .
Соотношение неопределенностей (3.13.10) является одним из фундаментальных положений квантовой теории. Одного этого соотношения достаточно, чтобы получить ряд важных результатов, в частности:
1. Невозможно состояние, в котором частица находилась бы в состоянии покоя.
2. При рассмотрении движения квантового объекта необходимо во многих случаях отказаться от самого понятия классической траектории.
3. Часто теряет смысл деление полной энергии E частицы (как квантового объекта) на потенциальную U и кинетическую K . В самом деле, первая, т. е. U , зависит от координат, а вторая - от импульса. Эти же динамические переменные не могут иметь одновременно определенного значения.
Лекция 3.14.
Уравнение Шрёдингера. Квантование энергии и момента импульса. Атом водорода.
Волновая функция. Уравнение Шрёдингера.
В развитие идеи де-Бройля о волновых свойствах вещества Э.Шрёдингер получил в 1926г. свое знаменитое уравнение. Он сопоставил движению микрочастицы комплексную функцию координат и времени, которую назвал волновой функцией и обозначил греческой буквой . Поэтому ее называют также пси-функцией. Она характеризует состояние микрочастицы. Физический смысл водновой функции состоит в следующем: квадрат ее модуля определяет вероятность нахождения частицы в промежутке между точками х и х+dх в момент времени t. Точнее величина является плотностью вероятности или плотностью распределения координат частицы.
Из такого определения следуют свойства волновой функции. Она должна быть однозначной, непрерывной, гладкой (производная не терпит разрыва), конечной. Кроме того, она должна подчиняться условию нормировки .
Основная задача физики микрочастиц (волновой или квантовой механики) как раз и состоит в нахождении волновых функций и связанных с ними физических следствий в самых разнообразных условиях. Для ее решения служит волновое уравнение Шрёдингера – основное уравнение нерелятивистской квантовой механики. (Заметим, что одним из решений этого уравнения в свободном пространстве должна быть плоская волна де-Бройля (3.13.9).)
Особое значение в квантовой механике имеют стационарные состояния. Это такие состояния, в которых все наблюдаемые физические параметры не меняются с течением времени. Оказывается, что в стационарных состояниях
![]() , (3.14.1)
, (3.14.1)
где частота постоянна, а функция не зависит от времени. Эта независящая от времени часть волновой функции может быть найдена из уравнения Шрёдингера для стационарных состояний
 , (3.14.2)
, (3.14.2)
где т - масса частицы, Е – ее энергия, - функция, которая в случае стационарных состояний имеет смысл потенциальной энергии частицы.
Энергия частицы Е входит в уравнение в качестве параметра. В теории дифференциальных уравнений доказывается, что уравнения вида (3.14.2) имеют решения, удовлетворяющие стандартным условиям, не при любых значениях параметра Е, а лишь при некоторых избранных значениях. Эти избранные значения называются собственными значениями энергии. Решения (значения волновой функции), соответствующие собственным значениям Е , называются собственными функциями. Совокупность собственных значений называется спектром величины (энергии). Если эта совокупность образует дискретную последовательность, спектр называется дискретным, если же – непрерывную последовательность, спектр непрерывный или сплошной.
Таким образом, из основных положений квантовой механики без каких-либо дополнительных предположений следует квантование (дискретность) энергии .
Частица в бесконечно глубокой потенциальной яме.
Рассмотрим квантование энергии на простейшем примере движения частицы, находящейся в бесконечно глубокой одномерной потенциальной яме. Пусть частица может двигаться только вдоль оси х, где движение ограничено непроницаемыми для частицы стенками: х = 0 и х = l. Потенциальная энергия рана нулю при 0≤ х ≤ l и обращается в бесконечность при х < 0 и x > l .
Поскольку волновая функция в этом случае будет зависеть только от х , уравнение Шрёдингера будет иметь вид
![]() . (3.14.3)
. (3.14.3)
За пределы потенциальной ямы частица попасть не может. Поэтому вероятность обнаружить там частицу, а, следовательно, и волновая функция в этих областях равна нулю. Из условия непрерывности следует, что и на границах ямы она равна нулю
![]() . (3.14.4)
. (3.14.4)
В области, где не равна тождественно нулю, уравнение (3.14.3) примет вид ![]() . (3.14.5)
. (3.14.5)
Введя обозначение , (3.14.6)
получим уравнение ![]() , (3.14.7)
, (3.14.7)
решение которого будет иметь вид
Из первой части условия (3.14.4) следует . Вторая часть этого условия ![]()
Будет выполнена лишь в случае, если
(n= 1,2,3,…), (3.14.9)
откуда, приняв во внимание (3.14.6), найдем собственные значения энергии частицы ![]() (п=
1,2,3,…). (3.14.10)
(п=
1,2,3,…). (3.14.10)
Спектр энергии оказался дискретным.
Оценим «расстояния» между соседними уровнями. Разность энергий между двумя соседними уровнями равна
Если оценить эту величину для молекулы газа в сосуде (т ~ 10 кг, l ~ 10cм), получим Дж эВ. Столь густо расположенные энергетические уровни будут практически восприниматься как сплошной спектр энергии, так что, хотя квантование энергии в принципе будет иметь место, на характере движения молекул это сказываться не будет. Аналогичный результат получим, если рассмотреть поведение свободных электронов в металле (те же размеры ямы, т ~ 10 кг, Дж эВ). Однако, совсем другой результат получится для электрона, если область, в пределах которой он может двигаться, будет порядка атомных размеров (~ 10 м). В этом случае
так что дискретность энергетических уровней будет весьма заметна.
Атом водорода.
Рассмотрим систему, называемую водородоподобным атомом, состоящую из неподвижного ядра с зарядом Ze и движущегося вокруг него электрона (при Z=1 – это атом водорода). Потенциальная энергия электрона представляет собой в этом случае сферически симметричную функцию
Такой случай не предусматривался теорией Бора. В ней движение электрона вокруг ядра происходило по плоским орбитам. Но в квантовой механике, в которой нет представления о движении электронов по орбитам, нет препятствий для реализации сферически симметричных состояний атома. Поэтому уравнение Шрёдингера целесообразно записать в сферической системе координат: r, .
Решая это уравнение, получим, что собственные значения энергии могут принимать 1)любые положительные значения 2) дискретные отрицательные значения, равные ![]() (п=
1,2,3,…). (3.14.13)
(п=
1,2,3,…). (3.14.13)
Случай Е > 0 соответствует электрону, пролетающему вблизи ядра и удаляющемуся на бесконечность. Случай Е < 0 - электрону, связанному с ядром. Заметим, что полученное выражение (3.14.13) совпадает с соответствующей формулой теории Бора (3.12.12). Однако в квантовой механике эти значения получаются из решения основного уравнения без введения каких-либо дополнительных предположений.
Собственные функции уравнения Шрёдингера оказываются от трех целочисленных параметров, которые принято обозначать п, l, т , и распадаются на два множителя, один из которых зависит только от r , другой – от углов
Параметры п, т называются квантовыми числами. Параметр п называется главным квантовым числом и совпадает с номером уровня энергии в (3.14.13). Параметр l называется азимутальным (или орбитальным) квантовым числом и может при заданном п принимать значения
Электрон в атоме водорода
Постулаты Бора
Постулаты Бора определили направление развития новой науки – квантовой физики атома. Но они не содержали рецепта определения параметров стационарных состояний (орбит) и соответствующих им значений энергии E n .
Правило квантования, приводящее к согласующимся с опытом значениям энергий стационарных состояний атома водорода, Бором было угадано. Он предположил, что момент импульса электрона, вращающегося вокруг ядра, может принимать только дискретные значения, кратные постоянной Планка. Для круговых орбит правило квантования Бора записывается в виде
![]()
Здесь m e – масса электрона, υ – его скорость, r n – радиус стационарной круговой орбиты. Правило квантования Бора позволяет вычислить радиусы стационарных орбит электрона в атоме водорода и определить значения энергий. Скорость электрона, вращающегося по круговой орбите некоторого радиуса r в кулоновском поле ядра, как следует из второго закона Ньютона, определяется соотношением
где e – элементарный заряд, ε 0 – электрическая постоянная. Скорость электрона υ и радиус стационарной орбиты r n связаны правилом квантования Бора. Отсюда следует, что радиусы стационарных круговых орбит определяются выражением
Самой близкой к ядру орбите соответствует значение n = 1. Радиус первой орбиты, который называется боровским радиусом, равен

Радиусы последующих орбит возрастают пропорционально n 2 .
Полная механическая энергия E системы из атомного ядра и электрона, обращающегося по стационарной круговой орбите радиусом r n , равна

Следует отметить, что E p < 0, так как между электроном и ядром действуют силы притяжения. Подставляя в эту формулу выражения для υ 2 и r n , получим:

Целое число n = 1, 2, 3, ... называется в квантовой физике атома главным квантовым числом.
Согласно второму постулату Бора, при переходе электрона с одной стационарной орбиты с энергией E n на другую стационарную орбиту с энергией E m < E n атом испускает квант света, частота ν nm которого равна ΔE nm / h:
Эта формула в точности совпадает с эмпирической формулой Ридберга для спектральных серий атома водорода, если положить постоянную R равной
Подстановка числовых значений m e , e, ε 0 и h в эту формулу дает результат
R = 3,29·10 15 Гц, который очень хорошо согласуется с эмпирическим значением R. Рис. 1 иллюстрирует образование спектральных серий в излучении атома водорода при переходе электрона с высоких стационарных орбит на более низкие.

Электрон в атоме водорода
Потенциальная энергия взаимодействия электрона с ядром в атоме водорода равна
Решение уравнения (1.15) проводят методом разделения переменных с учетом естественных требований, налагаемых на ψ -функцию: она должна быть однозначной, конечной, непрерывной и гладкой. В теории дифференциальных уравнений доказывается, что решения уравнения являются непрерывными, однозначными и конечными в следующих случаях:
1) при любых положительных непрерывных значениях энергии;
2) при дискретных отрицательных значениях энергии.
Первый случай соответствует свободному электрону (заштрихованная область на рис. 1.5 б ), второй - получаемым из уравнения Шрёдингера собственным значениям энергии
| | (1.16) |
Случай (Е < 0) соответствует связанным состояниям электрона в атоме.
Решение уравнения Шрёдингера приводит в случае Е < 0 к формуле (1.16) для энергетических уровней без использования каких-либо дополнительных постулатов (в отличие от первоначальной теории Бора). Кроме того, совпадение с формулой Бора означает, что мы пришли к той же самой системе энергетических уровней, как в теории Бора. Это же относится и к частотам излучения при переходах между уровнями.
Таким образом, решение уравнения Шрёдингера приводит для атома водорода к появлению дискретных энергетических уровней Е 1 , Е 2 , ..., Е п, показанных на рис. 1.5 б в виде горизонтальных прямых.


а ) б )
Рис. 1.5 . а - потенциальная энергия U(r) и б - собственные значения энергии Е электрона в атоме водорода.
Самый нижний уровень Е 1 , отвечающий минимальной возможной энергии, - основной , все остальные (Е п > Е 1 , п = 2, 3, ...) - возбужденные . При Е < 0 движение электрона является связанным - он находится внутри гиперболической потенциальной ямы. Из рисунка следует, что по мере роста главного квантового числа п энергетические уровни располагаются теснее и при п → ∞ Е ∞ → 0.
При Е > 0 движение электрона является свободным ; область непрерывного спектра Е > 0 (заштрихована на рис. 1.5 б ) соответствует ионизированному атому.
Различие в интерпретации с теорией Бора относится только к состояниям электрона: в теории Бора это движение по стационарным орбитам, здесь же орбиты теряют физический смысл, их место занимают ψ -функции.
Диаграмма энергетических уровней (рис.1.5) позволяет дать несколько важных определений.
Энергия возбуждения Е воз – это энергия, которую необходимо сообщить электрону, чтобы он из основного состояния (n = 1) перешёл в возбужденное. Например, Е воз = 10,2 эВ – энергия, необходимая для перехода электрона в состояние, соответствующее n = 2 (первое возбужденное состояние).
Энергия ионизации Е ион – энергия, необходимая для отрыва электрона, находящегося в основном состоянии (n = 1), от ядра, т.е. для перевода электрона на уровень с n = ∞ . Для атома водорода энергия ионизации равна 13,6 эВ.
Из анализа следует три вывода.
· Э лектрон в атоме может иметь только дискретные значения энергии. В любом атоме энергии электронов дискретны.
· Существует состояние электрона с энергией, меньше которой электрон иметь не может. Это состояние называется основным. Все остальные состояния называют возбужденными. При этом, двигаясь с ускорением, любая заряженная частица излучает электромагнитные волны. На этом принципе устроены все антенны, любые источники электромагнитного излучения - радиоволн, видимого света, рентгеновских и гамма-лучей. А электрон в атоме, в каком бы состоянии он ни находился, не излучает, хотя движется с ускорением. Электрон в возбужденном состоянии может излучить электромагнитную энергию, перейдя в одно из состояний с меньшей энергией. Энергия излучается квантами, и в процессе излучения, как во всех процессах, происходящих в природе, выполняется закон сохранения энергии. Энергия излученного кванта в соответствии с законом сохранения энергии равна hn = = E n - E m , где n и m - целые числа и n > m . Сколько времени электрон проведет в возбужденном состоянии, зависит от целого ряда причин, исследованных квантовой механикой. Эти времена различны, но все они конечны.
· Как исключение, основное состояние электрона в атоме устойчиво, поскольку закон сохранения энергии запрещает электрону, находящемуся в основном состоянии, излучать электромагнитную энергию.




